Prémio Nobel da Química 2013
📧
- DQB/LAQV/Universidade do Porto
Referência Fernandes, P.A., (2013) Prémio Nobel da Química 2013, Rev. Ciência Elem., V1(1):002
DOI http://doi.org/10.24927/rce2013.002
Palavras-chave Nobel; química; enzima;
Resumo
O prémio Nobel da Química de 2013 foi atribuído a três cientistas, Martin Karplus, Arieh Warshel e Micheal Levitt, a desenvolver investigação essencialmente (mas não exclusivamente) nos Estados Unidos.
Os três cientistas realizaram a sua investigação na área da química teórica e computacional, com ênfase na simulação computacional de proteínas e enzimas.
De acordo com a Academia Sueca, o fundamento do prémio foi “The development of multiscale models for complex chemical systems”.
O que é que esta frase quer dizer exatamente? O que são os modelos multiescala? O que são sistemas químicos complexos?
O problema fundamental que se deparava a estes cientistas era a simulação de reações químicas catalisadas por enzimas. As enzimas são os sistemas químicos complexos.
Mas o que têm de complexo as enzimas, do ponto de vista de simulação computacional?
A dificuldade em simular a catálise enzimática reside no facto de as enzimas serem moléculas de muito grande dimensão (geralmente com dezenas de milhares de átomos), possuindo um pequeno local (denominado o centro ativo) onde se dão reações químicas, sendo lá o substrato (o reagente) convertido no produto. O centro ativo e o substrato são compostos por umas meras dezenas/centenas de átomos, sendo que a restante parte da enzima (milhares/dezenas de milhar de átomos) serve para criar interações eletrostáticas que catalisam a reação química no centro ativo.
Esta situação é altamente complexa do ponto de vista computacional, porque para simular reações químicas precisamos obrigatoriamente de descrever o sistema à escala do eletrão, através da mecânica quântica (gerando cálculos extremamente complexos), mas para descrever as interações eletrostáticas do remanescente da enzima não podemos recorrer à mesma mecânica quântica, uma vez que a sua vasta dimensão gera cálculos quase irresolúveis
A solução encontrada para tratar o remanescente da enzima foi regredir a uma descrição mais simples, à escala do átomo, usando mecânica clássica, para esta vasta região. Felizmente a mecânica clássica consegue prever com sucesso essas mesmas interações eletrostáticas.
Em resumo:
i) Precisamos da mecânica quântica para descrever qualquer fenómeno que implique rearranjos electrónicos significativos (tais como as reações químicas, que envolvem redistribuição dos eletrões de valência), mas a mecânica quântica gera cálculos tão complexos que nem o mais potente computador existente consegue resolver com exatidão para sistemas com mais do que umas centenas de átomos.
ii) Precisamos da mecânica clássica para descrever sistemas de grande dimensão, que podem conter até ao milhão de átomos. A mecânica clássica descreve-os corretamente desde que não tenham lugar rearranjos electrónicos significativos. De facto, na mecânica clássica os electrões e os núcleos não são individualizados, são tratados em conjunto num átomo indivisível. As interações entre átomos distantes de uma mesma molécula, ou entre moléculas vizinhas, são bem descritos pela mecânica clássica.
Ficamos assim com um sistema multiescala, um sistema com duas escalas neste caso. O centro ativo e substrato, pequenos, são descritos por mecânica quântica e o remanescente da enzima é descrito por mecânica clássica. A figura 1 ilustra esta situação.
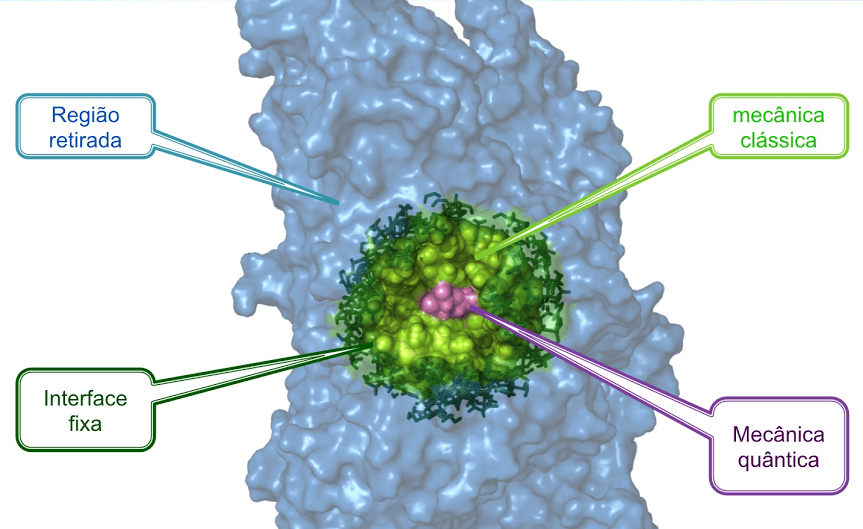
Quando se tem um sistema multiescala, o maior problema é a ligação entre as duas escalas. É como fazer a região descrita por mecânica quântica “sentir” e interatuar com a região descrita por mecânica clássica, e vice versa. Esse trabalho teve início no final dos anos 70, levado a cabo pelos laureados, e ainda é uma área de intensa investigação, com vários métodos disponíveis para o mesmo fim, cada um com as suas vantagens e desvantagens. Os métodos desenvolvidos pelos laureados foram os primeiros, os pioneiros, que mostraram que era possível fragmentar uma grande molécula entre duas descrições físicas, clássica e quântica, e fazê-las interatuar de forma exata, que reproduz com precisão a realidade. Por isso lhes foi atribuído o prémio Nobel.
O seu trabalho tem aplicação em muitos mais sistemas químicos, para além das enzimas, para os quais foi desenvolvido. De facto aplica-se a qualquer sistema químico que contenha uma molécula de grande dimensão, impossível de simular por mecânica quântica em toda a sua extensão, mas cujo fenómeno em estudo esteja essencialmente restrito a uma subregião pequena da mesma molécula.
Em Portugal existem diversos grupos de investigação a trabalhar nesta área, dos quais o grupo de investigação do autor deste artigo é apenas um exemplo.
Este artigo já foi visualizado 6134 vezes.



