Reação endotérmica
📧
- Faculdade de Ciências da Universidade do Porto
Referência Fernandes, R.F., (2015) Reação endotérmica, Rev. Ciência Elem., V3(3):177
DOI http://doi.org/10.24927/rce2015.177
Palavras-chave reação química; endotérmica; absorção; energia;
Resumo
Uma reação química é endotérmica se ocorre absorção de energia no decorrer da mesma.
No decorrer de uma reação química rompem-se ligações existentes nos reagentes e formam-se novas ligações que originam os produtos de reação. Durante o processo de rutura de ligações há sempre absorção de energia, e durante o processo de formação de ligações há sempre libertação de energia. Assim, a partir do balanço energético destes dois processos, verifica-se que nas reações químicas endotérmicas a energia absorvida para romper as ligações nos reagentes é maior que a energia libertada pela formação das ligações nos produtos de reação.
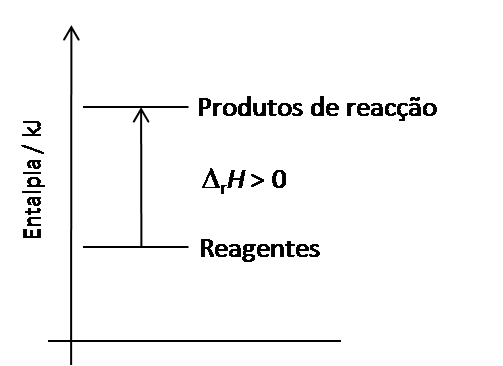
O termo endotérmico deriva do prefixo grego -endo que significa “dentro” e do sufixo grego -térmico, que significa “aquecer”.
A energia absorvida pelo sistema, aquando da reacção endotérmica, é transferida da vizinhança para o sistema, geralmente sob a forma de calor. Em condições de pressão constante, essa energia (calor absorvido) identifica-se com a variação de entalpia de reação \(\Delta\)rH). Assim, e dado que a maioria das reações estudadas no laboratório ocorrem em sistemas abertos, à pressão atmosférica (em condições de pressão constante), se há absorção de calor (reação endotérmica) a variação de entalpia é positiva.

Isto é, numa reação endotérmica a variação total da entalpia da reação, (\(\Delta\)rH), é positiva, dado que o somatório das entalpias de formação dos reagentes é menor do que o verificado para os produtos (figura 1).
Uma reação endotérmica bem conhecida é a que resulta da mistura de hidróxido de bário octa-hidratado (Ba(OH)2.8H2O) com tiocianato de amónio (NH4SCN). Quando se misturam estes dois reagentes, por exemplo, num gobelé verifica-se um arrefecimento acentuado nas paredes do mesmo.
Este efeito é semelhante ao que se observa nos sacos frios aplicados no tratamento de lesões desportivas, para o alívio da dor. Estes sacos consistem numa embalagem que se encontra dividida em duas frações através de uma membrana. Uma das frações contém água e a outra contém nitrato de amónio. Quando se utiliza o saco frio, rompe-se a membrana, as duas substâncias entram em contacto e ocorre um processo de dissolução/reação fortemente endotérmico, que ao absorver calor das vizinhanças faz baixar a temperatura das mesmas, ou seja, do próprio saco e portanto da zona lesionada.
Referências
- 1 http://goldbook.iupac.org/E02095.html, consultado em 16/01/2010.
- 2 http://antoine.frostburg.edu/chem/senese/101/glossary/e.shtml, consultado em 16/01/2010.
- 3 http://scienceworld.wolfram.com/chemistry/Endothermic.html, consultado em 16/01/2010.
Este artigo já foi visualizado 21742 vezes.



