Viscosidade
📧
- Universidade do Porto
Referência Lage, E., (2018) Viscosidade, Rev. Ciência Elem., V6(4):085
DOI http://doi.org/10.24927/rce2018.085
Palavras-chave Viscosidade; força; Newton; fluido;
Resumo
Uma propriedade universal dos fluidos e que se manifesta como uma força de atrito.
Qual a origem microscópica da viscosidade1? Recordemos a sua definição fenomenológica: para manter um fluido (gás ou liquido) em escoamento permanente entre dois planos (FIGURA 1), estando fixo um deles e movendo-se uniformemente o outro, é necessário aplicar uma tensão tangencial τ neste outro, originando-se, desta forma, um gradiente da velocidade \(\upsilon_X(y)\) o qual satisfaz à lei de Newton: \(\tau=\eta\frac{d\upsilon_x}{dy}\), onde η é o coeficiente de viscosidade do fluido. Somos, então, obrigados a concluir que esta é a tensão que se exerce em cada plano, paralelo aos anteriores, situado no interior do fluido, caracterizando a força tangencial, por unidade de área, que a parte do fluido acima do plano exerce sobre a parte abaixo do plano.
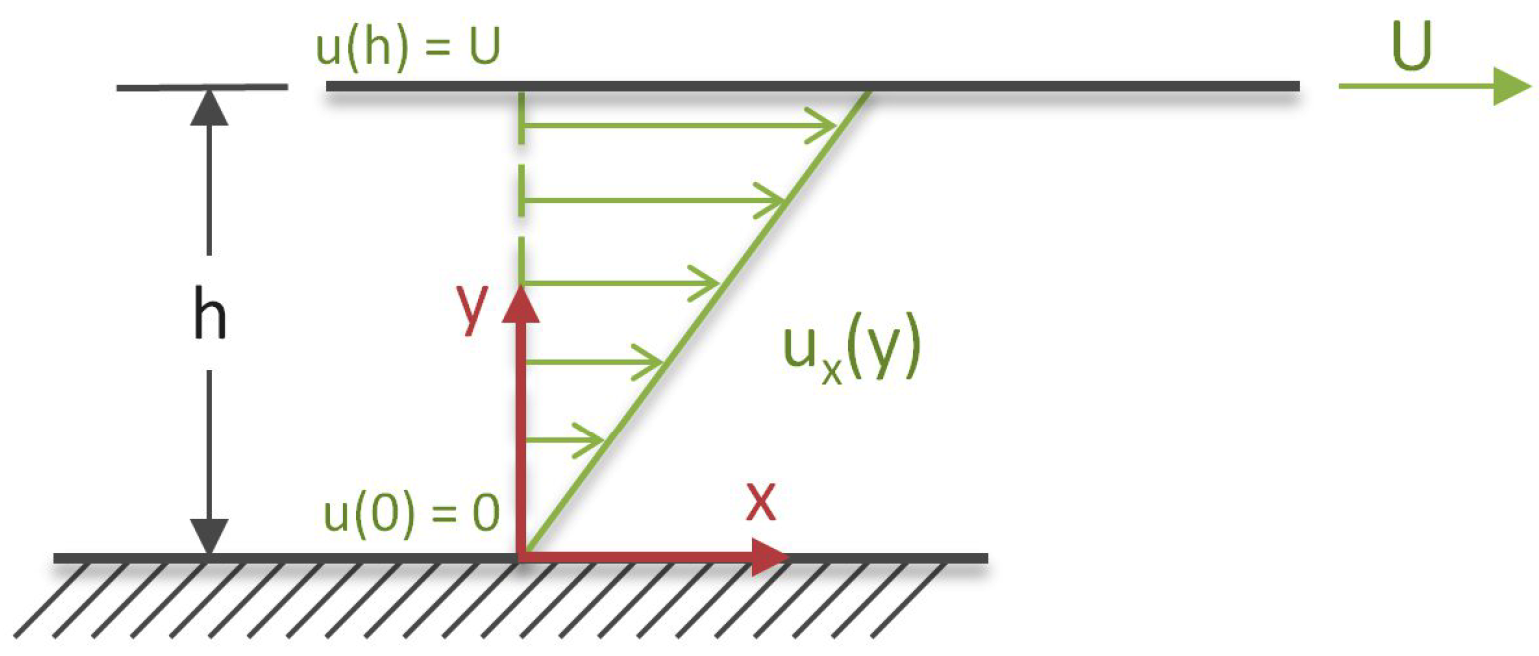
Comecemos por considerar um gás ou vapor, o que nos permite ignorar, em primeira aproximação, as forças intermoleculares. Considerando a FIGURA 1, as moléculas, em qualquer porção do fluido, têm uma velocidade macroscópica sobreposta à sua agitação microscópica. Imaginemos um plano horizontal no seio do fluido: há moléculas, abaixo deste plano, que passam, num curto intervalo de tempo, para cima, transportando uma quantidade de movimento ligeiramente menor (porque é menor a velocidade macroscópica) que a quantidade de movimento das moléculas acima do plano; no mesmo intervalo de tempo, igual2 número de moléculas atravessa o plano de cima para baixo, transportando uma quantidade de movimento ligeiramente maior do que a quantidade de movimento das moléculas abaixo do plano. Deste modo, o fluido acima do plano tende a diminuir a sua quantidade de movimento, i.e, experimenta uma força que o trava; enquanto o fluido abaixo do plano tende a aumentar a sua quantidade de movimento, i.e., experimenta uma força que o acelera. Baseando-nos nesta imagem, podemos deduzir uma expressão para o coeficiente de viscosidade. Consideremos a unidade de área num plano intermédio y qualquer da FIGURA 1. O número de partículas que, em cada segundo, atravessa esta área, de cima para baixo, é \(\frac{1}{4}n\langle \upsilon\rangle\), onde \(n\) é o número de partículas por unidade de volume e \(\langle \upsilon\rangle\) é a média da sua velocidade microscópica. Cada uma destas partículas, de massa \(m\), transporta a velocidade macroscópica \(\upsilon_x\) calculada, aproximadamente, em \(y + l\), onde \(l\) é o livre percurso médio (distância média entre colisões sucessivas). Portanto, a quantidade de movimento transferida, por unidade de área e de tempo, de cima para baixo é \(\frac{1}{4}n\langle \upsilon\rangle m\upsilon_x(y+l)\); de modo análogo, a quantidade de movimento transferida, por unidade de área e de tempo, de baixo para cima é \(\frac{1}{4}n\langle \upsilon\rangle m\upsilon_x(y-l)\). Então, o ganho de quantidade de movimento, por unidade de área e de tempo, da parte do fluido abaixo do plano é a diferença destas duas quantidades, i.e., a tensão tangencial exercida pela parte acima do plano sobre a parte abaixo do plano é \(\tau\cong\frac{1}{2}n\langle \upsilon\rangle ml\frac{d\upsilon_x}{dy}\), pelo que \(\eta\cong\frac{1}{2}n\langle \upsilon\rangle ml\). Assim, um aumento de pressão, que faz aumentar a densidade, ou um aumento de temperatura, que faz aumentar a velocidade microscópica e, portanto, aumenta o fluxo de partículas, levam a um aumento da viscosidade (FIGURA 2).
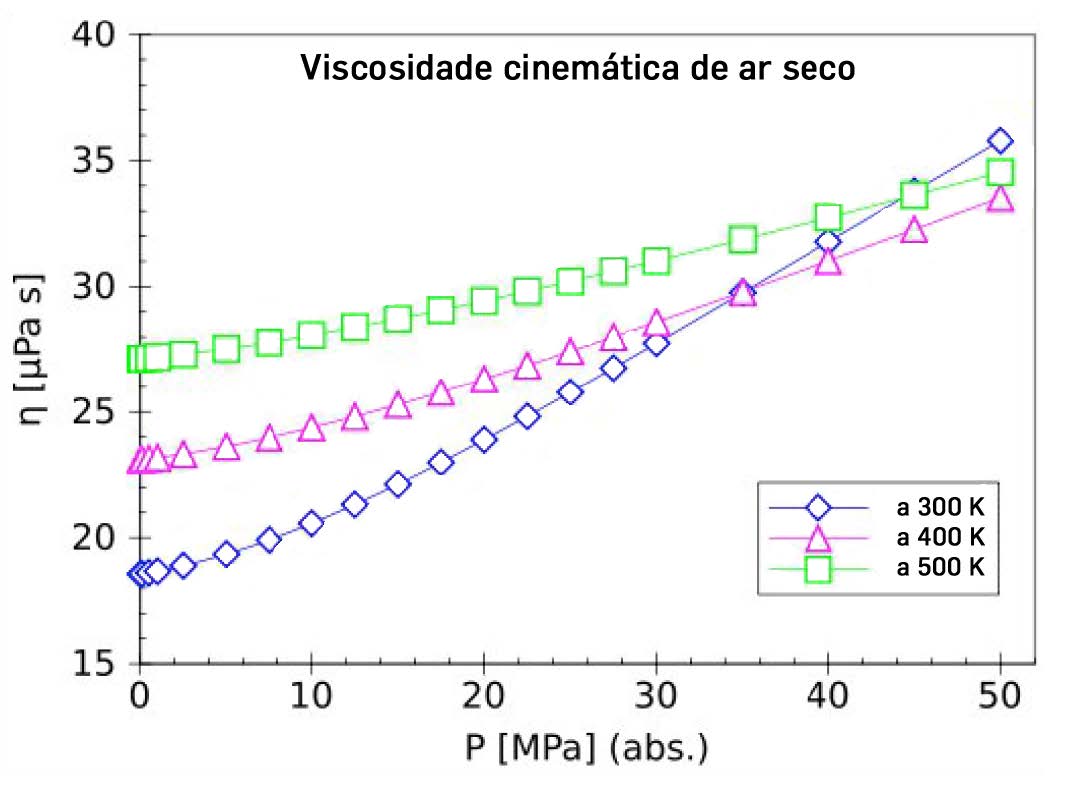
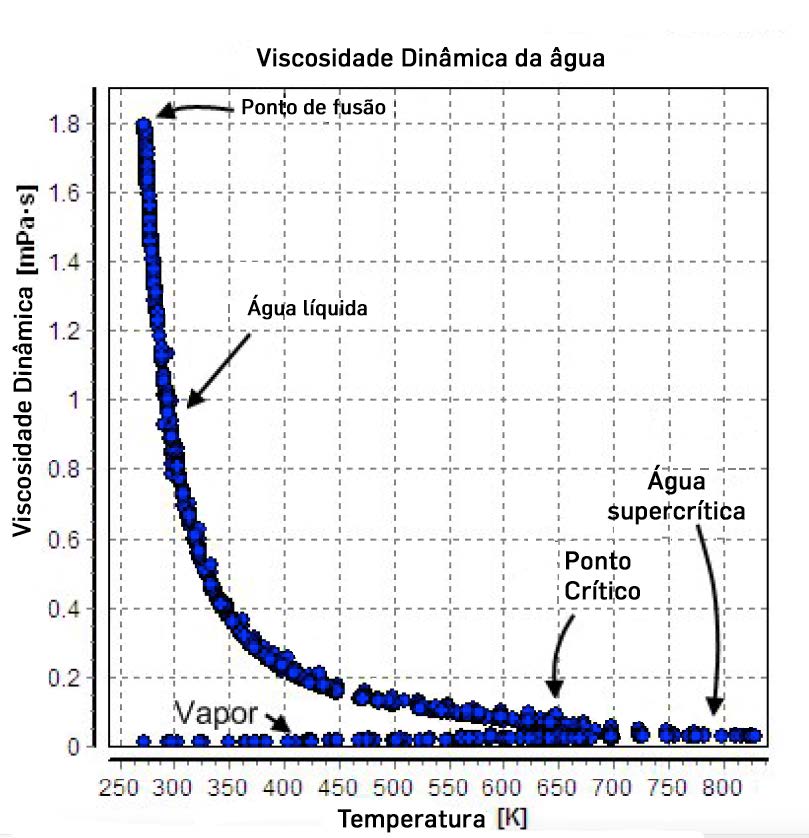
Num liquido, a explicação anterior mantém-se, mas não podemos ignorar as forças intermoleculares: a muito maior densidade de um liquido em relação a um gás, significa, por um lado, que é muito maior o número de moléculas a atravessar o plano imaginado, pelo que é muito maior a viscosidade do líquido do que a de um gás, e, por outro lado, justifica que o efeito da pressão na viscosidade seja diminuto, porque um líquido é praticamente incompressível. Porém, um aumento de temperatura, se aumenta, como num gás, o fluxo de partículas, tem, como contrapartida, uma diminuição da importância do potencial intermolecular em relação à energia cinética microscópica, levando o liquido a ter um comportamento mais parecido com o de um gás, i.e., diminuindo a sua viscosidade (FIGURA 3). Note-se a diferença das escalas da viscosidade neste dois gráficos.
Notas:
1Ver “Fluidos”.
2O número de moléculas que atravessa o plano num e noutro sentido, durante o mesmo curto intervalo de tempo, é estatisticamente o mesmo porque não há transporte macroscópico de massa através do plano.
Referências
- 1 Massey, B. S., Ward-Smith, A. J., Mechanics of Fluids (9th ed.). London & New York: Spon Press, 2011. ISBN 978-0-415-60259-4. OCLC 690084654
- 2 Tritton, D.J., Physical fluids dynamics. New York: Van Nostrand-Reinhold, 1977.
- 3 J.F. DOUGLAS, J.M. GASIOREK, J.A. SWAFFIELD, Fluid Mechanics, Longman Scientific & Technical, Essex, 1995.
- 4 Lamb, W. Hydrodynamics.
- 5 Lai, W. M. et al., Introduction to continuum mechanics. Butterworth-Heinemann, 2009.
- 6 Prandtl, L., & Tietjens, O. G., Applied Hydrodynamics.
- 7 CURLE, N., DAVIES, H. J., Modern fluid dynamics, 1968.
- 8 Fetter, A. L., & Walecka, J. D., Theoretical mechanics of particles and continua. Courier Corporation, 2003.
Este artigo já foi visualizado 6248 vezes.



