Separar para conhecer
Cromatografia, um processo físico-químico de separação de moléculas
📧 , 📧
- * DEQ/ CERES/ FCTUC/ U. Coimbra
- ɫ DEQ/ CERES/ FCTUC/ U. Coimbra
Referência Braga, M. E. M., Matos, P., (2026) Separar para conhecer, Rev. Ciência Elem., V14(1):003
DOI http://doi.org/10.24927/rce2026.003
Palavras-chave
Resumo
A cromatografia é uma técnica que permite separar os diferentes componentes de uma mistura complexa, funcionando como um “filtro seletivo” que distingue moléculas com base nas suas propriedades físico-químicas. Este artigo apresenta uma introdução clara aos conceitos de fase móvel e estacionária, clarifica as diferentes tipologias de cromatografia segundo a sua geometria e mecanismo, e explica a interpretação de perfis de separação (cromatogramas). Finalmente, demonstra-se a utilidade prática da técnica na indústria alimentar, recorrendo a exemplos reais como a caracterização aromática de vinhos e a monitorização de contaminantes, essenciais para garantir a segurança do consumidor.
A origem da cromatografia remonta ao início do século XX, sendo atribuída ao botânico Mikhael Tswett, que utilizou a técnica para separar pigmentos vegetais, como as clorofilas1.
Desde então, evoluiu de um método simples de laboratório para uma das ferramentas analíticas mais poderosas da ciência moderna. Através dela, é possível identificar (análise qualitativa) e medir (análise quantitativa) substâncias em concentrações extremamente baixas, sendo indispensável em áreas que vão da medicina forense ao controlo de qualidade industrial.
Princípios básicos: o jogo das duas fases.
Para compreender a cromatografia, deve-se imaginar um sistema composto por duas fases:
Fase estacionária: um material que permanece fixo (pode ser um sólido ou um líquido retido num suporte).
Fase móvel: um fluido (líquido ou gás) que transporta a mistura a separar através da fase estacionária2.
A separação ocorre porque cada componente da mistura interage de forma diferente com estas duas fases3. As moléculas que têm maior “afinidade” pela fase estacionária movem-se mais lentamente, enquanto as que preferem a fase móvel avançam mais depressa4. Esta diferença de velocidade é o que permite a separação física dos componentes ao longo do tempo ou do espaço.
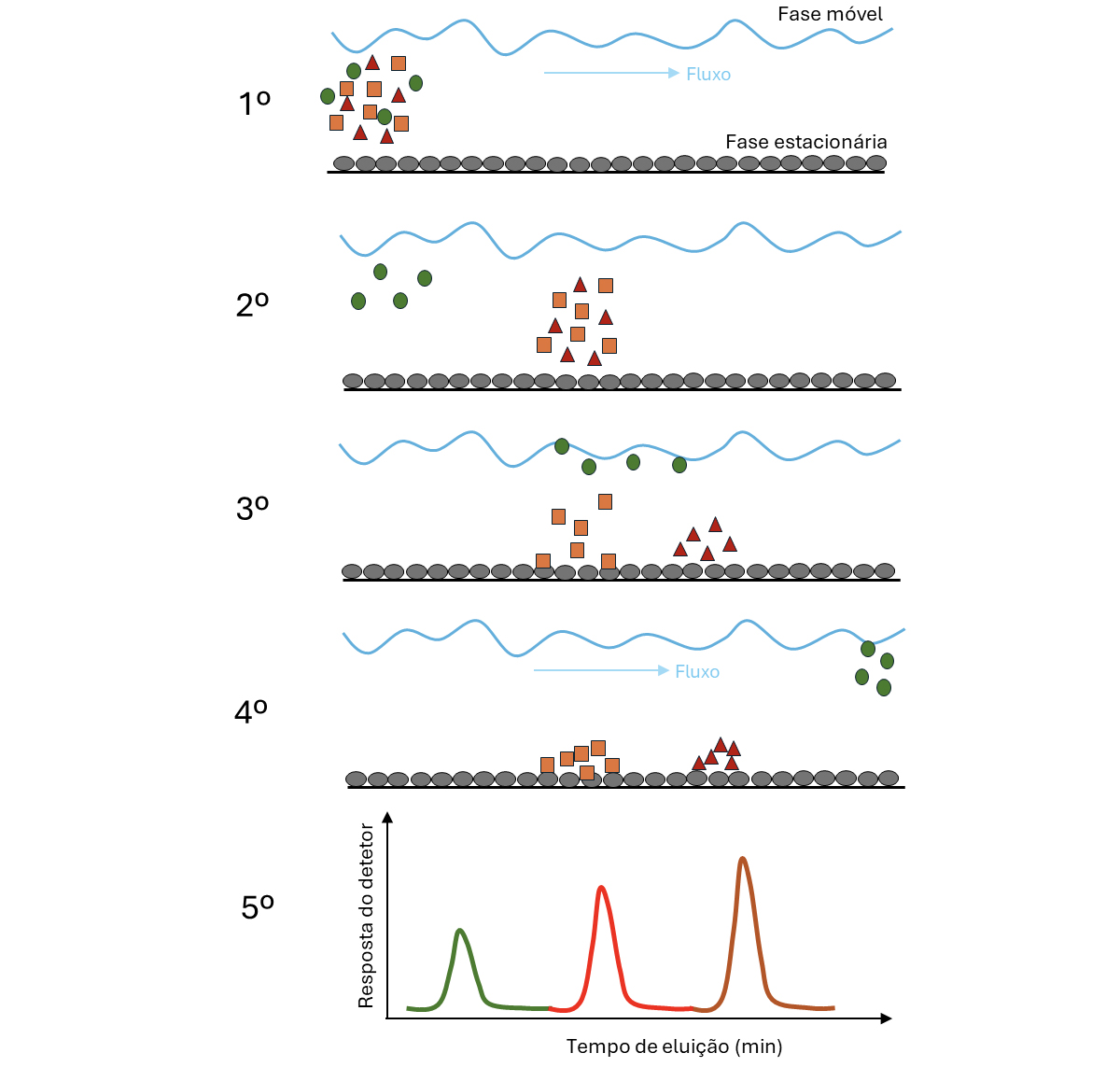
A FIGURA 1 representa o processo de forma simplificada: 1.º, a mistura é inserida no sistema; 2.º, a fase móvel transporta as moléculas que estabelecem um equilíbrio com a fase estacionária; 3.º e 4.º, sucessivas etapas de equilíbrio separam as moléculas consoante a sua afinidade; 5.º, o gráfico (cromatograma) mostra o sinal do detetor com a sequência de saída das moléculas.
Classificação e mecanismos (clarificação técnica).
Para evitar confusões comuns, é importante distinguir a geometria do sistema do mecanismo químico de interação5:
Quanto à geometria e fase móvel (TABELA 1):
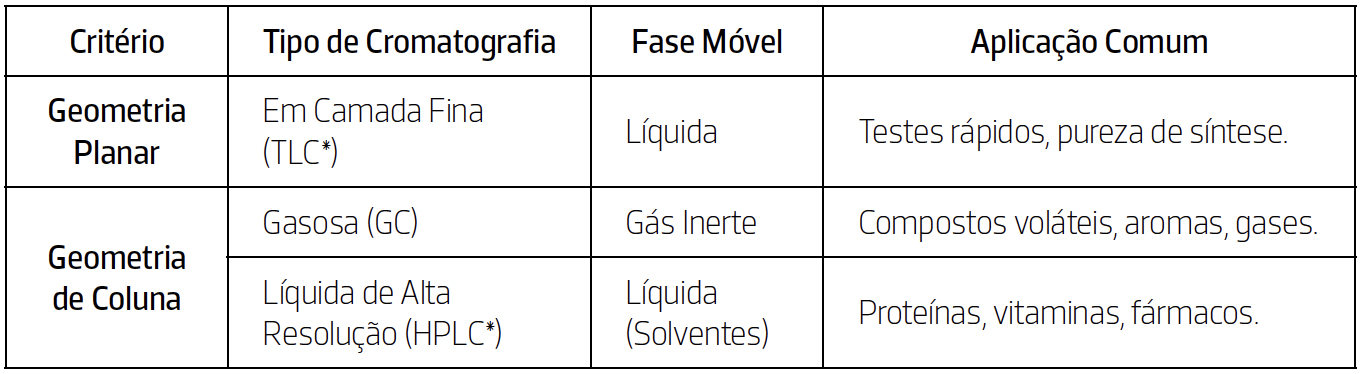
*TLC - do inglês Thin Layer Chromatography; HPLC – do inglês High Pressure Liquid Cromatography.
Cromatografia planar: realizada em superfícies planas, como papel ou placas de sílica (Cromatografia em Camada Fina).
Cromatografia em coluna: a fase estacionária está contida dentro de um tubo (coluna). Dependendo da fase móvel, divide-se em:
Cromatografia líquida (LC, do inglês Liquid Cromatography): usa solventes líquidos.
Cromatografia gasosa (GC, do inglês Gas Cromatography): usa gases inertes (ideal para substâncias voláteis).
A FIGURA 2 apresenta exemplos visuais dos materiais usados para as geometrias usadas.

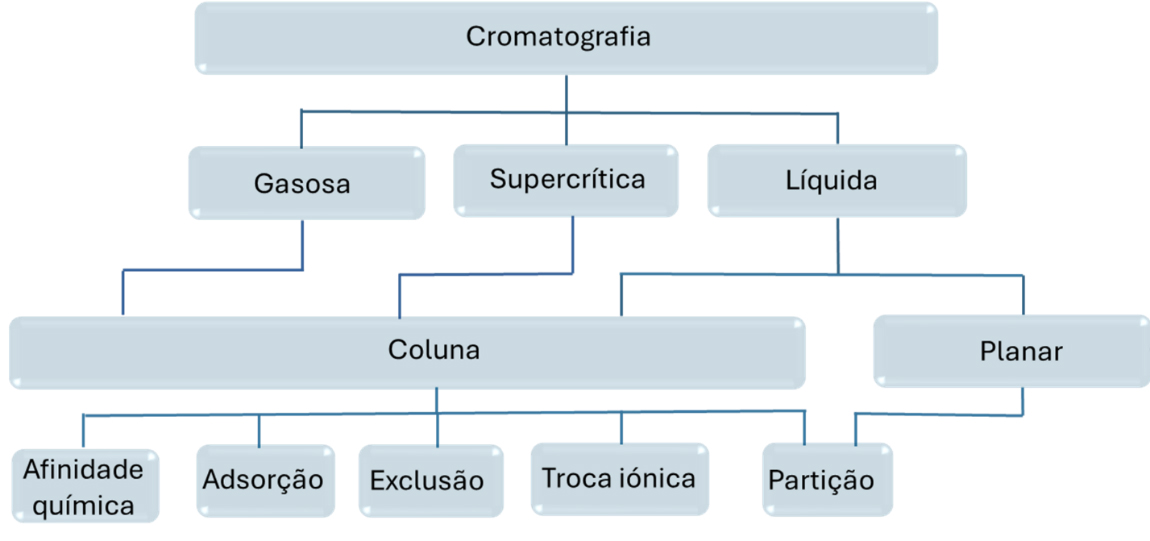
Quanto ao mecanismo de separação (o processo molecular), independentemente de ser em coluna ou planar, a separação pode ocorrer por:
Afinidade: baseada em interações biológicas específicas (ex: anticorpo-antigénio).
Adsorção: o analito adere à superfície da fase estacionária sólida4, 5, 6.
Exclusão molecular: as moléculas são separadas pelo seu tamanho, como um peneiro.
Troca iónica: baseada na atração entre cargas elétricas opostas.
Partição: o analito distribui-se entre a fase móvel e uma película líquida na fase estacionária (baseado na solubilidade)5, 6.
A FIGURA 3 apresenta essa classificação de forma simplificada.
Tempo de retenção (tR): o tempo que uma molécula demora a atravessar o sistema (correr pela coluna ou pela placa). É característico de cada substância (identidade).
Área do pico ou da mancha: é proporcional à quantidade de substância presente (quantidade).
Resolução (Rs): mede quão bem dois picos ou manchas estão separados. Uma boa resolução é crítica para garantir que um contaminante não está “escondido” sob o pico ou mancha de outro componente.
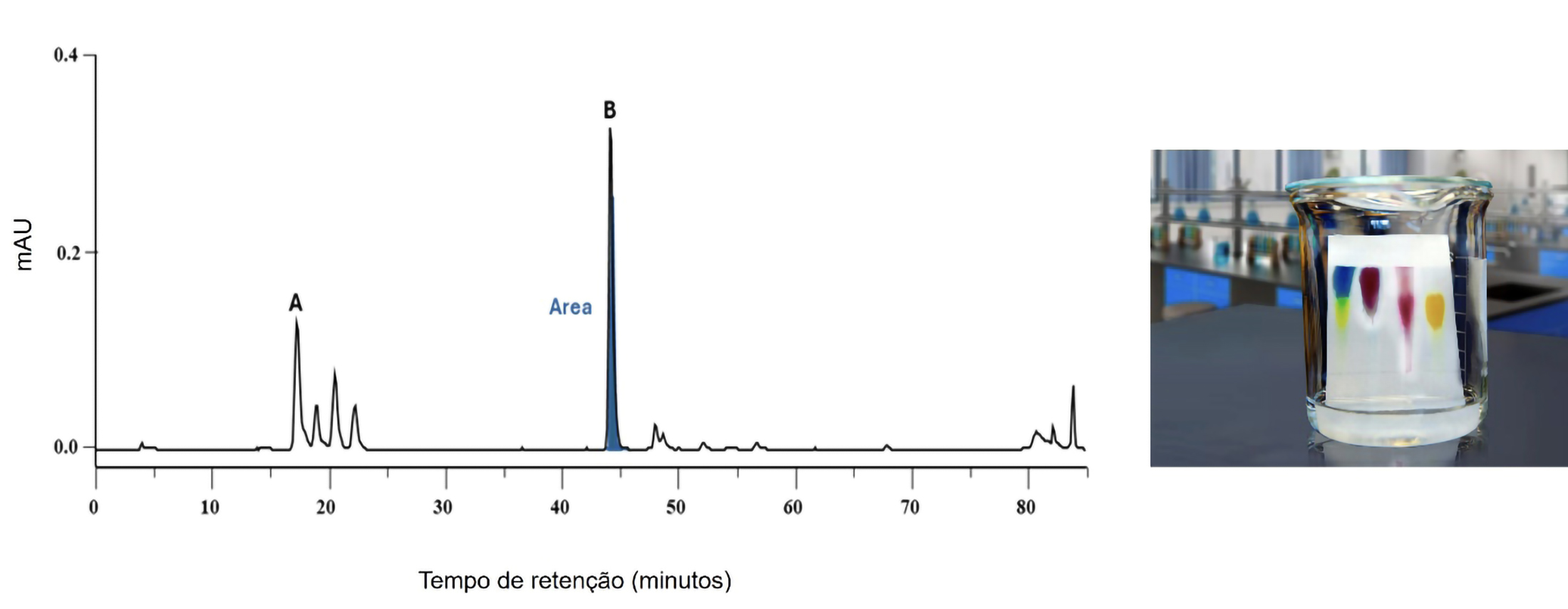
A FIGURA 4 apresenta um cromatograma feito em coluna, com picos bem separados e em destaque um pico com a área em azul para exemplificar. Também apresenta uma imagem de TLC, com manchas sobrepostas à esquerda, amarela e azul, e as arroxeadas - uma separada e outras que se arrastam com grande afinidade com a placa, e a última alaranjada com boa resolução.
Aplicações práticas e dados reais.
Autenticidade e aroma em vinhos.
Na vitivinicultura, a cromatografia é usada para definir o perfil sensorial7.
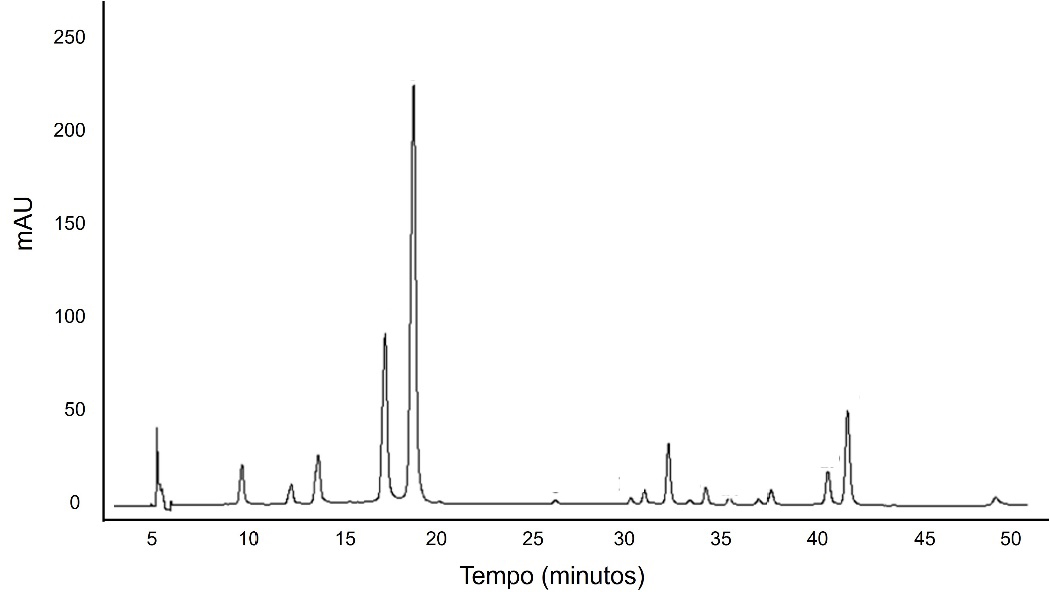
Estudos reais com vinhos da casta Aragonez utilizam a cromatografia gasosa (GC) para identificar picos de moléculas como a β-damascenona (aroma floral/frutado)8. Além disso, a técnica de HPLC permite identificar até 20 antocianinas diferentes9. Um cromatograma real de um vinho autêntico funciona como uma “impressão digital” (FIGURA 5); qualquer alteração nestes picos pode indicar a fraude por mistura com uvas de menor qualidade10.
Segurança alimentar: contaminantes e toxinas.
A legislação da União Europeia (UE) é rigorosa quanto a contaminantes11. A monitorização de segurança alimentar assenta na capacidade da cromatografia de detetar “vestígios” (quantidades ínfimas). Exemplos reais incluem:
PFAS (poluentes eternos): a cromatografia líquida permite detetar estes compostos químicos em águas e alimentos.
Alcaloides pirrolizidínicos: toxinas naturais em chás ou mel10. No cromatograma, a precisão da área do pico garante que estes níveis estão abaixo dos limites legais impostos pela União Europeia, protegendo a saúde pública.
Conclusão.
A cromatografia é muito mais do que um processo físico-químico; é o “sentido da visão” da química moderna sobre misturas invisíveis a olho nu. Ao clarificar os seus mecanismos e aplicar a sua precisão em contextos reais como a segurança alimentar e a vitivinicultura, transformamos a teoria numa ferramenta de proteção e conhecimento. Separar é, de facto, o primeiro passo para conhecer a fundo o mundo que nos rodeia.
Agradecimentos.
Este trabalho foi realizado no âmbito do projeto INSTREAM (https://doi. org/10.54499/2023.13656.PEX) e do financiamento estratégico e programático para o centro de investigação Centro de Engenharia Química e Recursos Renováveis para a Sustentabilidade (CERES) (https://doi.org/10.54499/UID/00102/2025; https://doi.org/10.54499/ UID/PRR/00102/2025) concedido pela Fundação para a Ciência e Tecnologia, em Portugal.
Referências
- 1 AUTOR, Tswett and the Invention of Chromatography. Milestones in Chromatography, LCGC North America, 21, 458-467. . 2003.
- 2 CARRILHO, E. et al., Fluidos Supercríticos em Química Analítica. I. Cromatografia Com Fluido Supercrítico: Conceitos Termodinâmicos, Quim. Nova, Vol. 24, No. 4, 509-515. 2001.
- 3 IUPAC, Compendium of Chemical Terminology, 5th ed. International Union of Pure and Applied Chemistry, Online version 5.0.0. 2025.
- 4 GINGER, L. M. & JASON D. M., Measurement of Biological Materials, Chapter 5 in Clinical and Translational Science Principles of Human Research, 69-86. 2009.
- 5 MEYER, V. R., Practical High-Performance Liquid Chromatography, John Wiley & Sons, ISBN:9780470682180. 2010.
- 6 PREMNATH, S. M. & ZUBAIR, M., Chromatography. In: StatPearls [Internet], Treasure Island (FL): StatPearls Publishing. 2025.
- 7 FANALI, M. U. et al., Flavors and odors analysis. In Chemical Analysis of Food - Techniques and Applications, Ed. Y. Pico, 2nd Edition, Academic Press. 2020.
- 8 BOTELHO, I. et al., Evaluation of two quantitative gas chromatography–olfactometry methods for clonal red wines differentiation, Flavour and Fragrance Journal, 22: 414–420. 2007.
- 9 GARCIA-BENEYTEZ, F. L. & CABELLO, E., Revilla. Analysis of Grape and Wine Anthocyanins by HPLC-MS. J. Agric, Food Chem., 51, 5622- 5629. 2003.
- 10 KAROUI, R., Food authenticity and fraud. In Chemical Analysis of Food - Techniques and Applications, Ed. Y. Pico, 2nd Edition, Academic Press. 2020.
- 11 CAMPO, J. & PICÓ, Y., Emerging contaminants and toxins. In Chemical Analysis of Food - Techniques and Applications, Ed. Y. Pico, 2nd Edition, Academic Press. 2020.
Este artigo já foi visualizado 355 vezes.